Comment calcule-t-on ? ... son rejet en CO2 avec les carburants ?
par Pierre Celle
une approche qui part d'une consommation constatée de 4 L / 100 km ; puis qui calcule à partir des composants des carburants
l'émission de gaz carbonique
le terrible CO2
1 ... S'intéresser à la question .... c'est le point de départ
... d’abord connaître de façon précise la consommation de mon déplaçoir !!
golfus deuxius dieselius dite golf 2 VW !! 
Avec une méthode précise .... c'est mieux !
( un brevet bien à ouam )
... enfin oui j'ai découvert que pour savoir il faut compter avec précision !
C'est à peu près comme si votre compteur de vitesse vous disait vous allez vers 70 km / h ( de 60 à 80 ) pas mal !
mais " peut mieux faire "
golfus deuxius dieselius a parcouru 195 km avec 6,5 L de GO !
= 3,33 L aux 100

2 ... Quantifier correctement " masse n'égale pas volume "
la masse volumique se note ρ
ρGO désigne la masse volumique du gazoil
ρGO = 850 kg/m3 ( 1 m3 de gazoil ; a une masse de 850 kg )
soit 3,33 * 0,85 = 2,83 kg de GO / 100 km
3 ... Allons plus loin avec et quel que soit le carburant ! [ il y a toujours 85% de C ]
vous ne me croyez pas ? 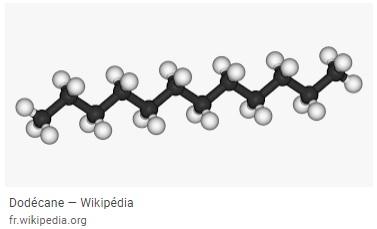
pourquoi quel que soit le carburant ?
... tout simplement parce que si je choisis le gazole pétrolier;
sa formule chimique moyenne est C12H24
( allant en réalité approximativement de C10H22 à C15H28 )
"les atomes de carbone en noir devraient être plus gros"
La voila en photo la molécule C12 H26
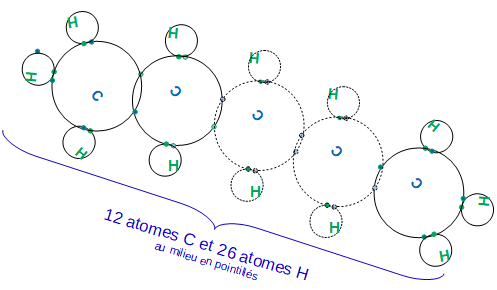
c'est donc [ un dodé cane " dodé 12 ; cane (alcane) ]
un alcane a toujours comme formule CnH2n+2
ça fait une petite chenille
.... ci-contre j'ai iréalisé un dessin qui respecte l'échelle des
grandeurs pour les atomes
4 ... Faisons un calcul quant à la proportion de carbone " puisque c'est lui qui produit CO2"
C12 H 26 environ ce qui donne 12 * 12 + 26 * 1 = 144 + 26 = 170 g ( restes de chimie et de stoechiométrie !!! )
1 mole C c'est 12 g ; 1 mole H c'est 1 g les chimistes comptent en g !!
Conclusion :170 g de carburant contiennent 144 g de C soit 144 / 170 = 84,7 %
( proportion identiques quelque soit le carburant - diesel ou essence donnent des résultats très voisins - )
L'octane de l'essence donnerait C8H18 soit 8 * 12 + 18*1 = 114 g et 96 / 114 = 0.842 84.2 % !! voila qui est prouvé !
CQFD !!
... donc je retiens les carburants pétroliers 85 % C
2,83 * 0,847 = 2,39 kg C
…. et C + O2 CO2
…. et 12 g + 2*16 g 44 g de CO2
…. ainsi 1000 g C + …. O2 44 * 1000 / 12 = 3666 g de CO2
Cela signifie clairement qur 1 kg de C produit 3,666 kg de CO2 en brûlant !
… et que golfus produit 3,666 * 2,39 kg = 8,761 kg de CO2 en roulant 100 km
…. 87 g / km rien que ça ! … et c’est en dessous de 100 g !!!
5 ... l’important pour aller vite
masse CO2 = litrage ρgaz-oil proportion de C dans carburant * 3666
(kg) (m³ ) ( kg/m3 ) ( % ) ( %)
 850 85 3,666 2648,6 kg/m3
850 85 3,666 2648,6 kg/m3
un m3 de carburant (quel qu'il soit ) emet en brûlant 2648, 6 kg de CO2
ce qui correspond à 2648 g / L .... si vous parcourez 100 km avec 1 L vous êtes tr ès bon 26, 48 g CO2 / 100 km !
50 km 52,96 g33,3 km 79.84 g
25 km 107,12 g
Ajouter un commentaire